Giriş
Pozitron emisyon tomografisi (PET) ile miyokart perfüzyon görüntüleme, son yıllarda kullanımı giderek artan bir modalite olarak ortaya çıkmaktadır. Stres ile indüklenmiş miyokardiyal perfüzyon defektlerini göstermek koroner arter hastalarına (KAH) yaklaşımda önemli tanısal ve prognostik bilgiler sağlamaktadır. Bununla birlikte, PET perfüzyon görüntüleme ile miyokardiyal kan akımının ölçülmesi ve her gram doku başına dakikadaki kan akımının mililitre olarak gösterilebilmesi gibi kantitatif verilerin de sağlanabilmesi, anatomik bilgiler veren ve invaziv bir yöntem olan anjiyografinin yanında fonksiyonel görüntülemeye olan eğilimi artırmıştır (1). Miyokart PET perfüzyon görüntüleme ile ateroskleroz veya mikrovasküler dolaşım bozukluğunun erken safhalardan itibaren tespiti ve üç damar hastalığındaki dengeli kan akımı azalmasının gösterilmesi de mümkün olabilmektedir (2). Tek foton emisyon bilgisayarlı tomografik görüntülemeye (SPECT) göre rezolüsyon ve duyarlılığının daha yüksek olması, daha düşük radyasyon maruziyeti ve daha doğru atenüasyon düzeltmesi gibi pek çok avantaja sahiptir (3).
Amaç
Bu kılavuzun amacı, kantitatif miyokart PET perfüzyon görüntüleme protokollerinin standardizasyonunu sağlamak, görüntülerin yorumlanması için güncel tanı kriterleri önermek ve klinik uygulamalarına ilişkin bazı bilgileri uluslararası kılavuzlar ve güncel literatür eşliğinde sunmaktadır.
Genel Bilgiler ve Tanımlamalar
PET Görüntüleme Sistemleri
PET, harici bir dedektör kullanılarak in vivo radyonüklid dağılımını gösteren, fonksiyonel ve fizyolojik bilgiler sağlayan, kesitsel ve üç boyutlu görüntüleme imkanı tanıyan bir yöntemdir. SPECT sistemleri ile karşılaştırıldığında uzaysal rezolüsyonu daha iyi (4-6 mm), yüksek sayımlar elde edildiği için daha duyarlı ve atenüasyon düzeltmesi de daha doğrudur (4). Bu avantajlarından dolayı PET görüntüleme ile daha iyi bir kantitasyon sağlanabilmektedir (5). Miyokardiyal kan akımı, hakkında non-invaziv olarak kantitatif bilgiler edinilebilmesini sağlayan PET radyofarmasötiklerinin genelde yarı ömürleri çok kısadır ve siklotron veya jeneratör ürünüdürler (6).
Dinamik kardiyak PET görüntülemede, enjekte edilen radyoaktivitenin tamamı, kalpten ilk geçiş sırasında tarayıcının görüş alanı içinde olduğu için çok yüksek sayım oranlarına elde edilir. Fakat birkaç dakika sonra özellikle Oksijen-15 su (O-15 su) ve Rubidyum-82’nin (Rb-82) hem kısa yarı ömürleri hem de radyoaktivitenin tüm vücuda dağılımı nedeniyle sayım oranları oldukça
düşer (7). Dinamik bir taramada ilk geçiş sırasında tarayıcının görüş alanı içindeki radyofarmasötik miktarı, tipik bir F-18 florodeoksiglukoz (FDG) tüm vücut taramasına göre 20-40 kat daha yüksektir.
PET tarayıcıları iki boyutlu (2D) veya üç boyutlu (3D) olarak üretilebilmektedir. Dedektör halkaları bölmelerle (septalarla) ayrılmışsa 2D tarayıcı, bölmelerle ayrılmamışsa 3D tarayıcı olarak adlandırılır. Bu bölmeler, bir halkadaki dedektörler ile bitişik veya daha uzak halkalardaki dedektörler arasında meydana gelen tesadüfi olayları ve saçılımları azaltır. Bölmesiz 3D tarayıcılar, mevcut halkalar arasında meydana gelen tüm tesadüfi olaylara izin vererek dedektör başına hassasiyeti ve sayım oranını önemli ölçüde artırır, ancak diğer yandan saçılım ve tesadüfi olayları da artırır. Bununla birlikte, geliştirilmiş hassasiyetten kaynaklanan avantajlar, artan saçılım ve tesadüfi olaylardan kaynaklanan dezavantajlardan çok daha ağır basmaktadır. En yeni nesil PET/bilgisayarlı tomografi (BT) tarayıcıları artık septa ile donatılmamaktadır, çünkü gelişmiş dedektör teknolojisi, artan bilgi işlem gücü, güncel yeniden yapılandırma algoritmaları ve yazılım programları 3D PET tarayıcıda üretilen yüksek sayım oranlarının daha iyi yönetilmesine olanak tanır (5). Time of flight (TOF) teknolojisine sahip tarayıcılarda ise sinyal/gürültü oranı daha yüksek olacağı için, kardiyak perfüzyon görüntülemede görüntü kalitesinde artışı da beraberinde getirecektir (8).
PET tarayıcılarda en yaygın olarak bizmut germanyum oksit (BGO), gadolinyum oksiortosilikat, lutesyum oksiortosilikat (LSO) ve lutesyum-yitriyum oksiortosilikat (LYSO) gibi kristaller kullanılmaktadır. Dinamik kardiyak görüntüleme için BGO kristalleri kullanıldığında, radyoaktivitenin ilk geçişi sırasında 3D tarayıcıya göre daha yüksek sayımlar elde edilebildiği için 2D tarayıcılar tercih edilirdi. Günümüzde LSO ve LYSO dedektörleri ve silikon foton çoğaltıcı tüpler ve TOF teknolojisi ile donatılmış 3D tarayıcılı PET sistemleri, hızlı elektronik devreler sayesinde daha da yüksek sayım oranları elde edilmesine olanak sağlamaktadır. Yakın zamana kadar kristale düşen fotonları elektrik sinyallerine çevirmek için foton çoğaltıcı tüpler kullanılan PET cihazlarında, PET/manyetik rezonans (MR) sistemlerinin de ortaya çıkması ve manyetik alanda foton çoğaltıcı tüplerden yüksek verim alınamaması nedeniyle, silikon foton çoğaltıcı tüpler kullanılmaya başlanmıştır (9,10). Dijital PET sistemleri de voksel düzeyinde daha iyi sayım oranları ve kantitatif veriler elde edilmesine olanak sağlamaktadır (11).
Hibrit PET/BT ve PET/MR Sistemleri
Günümüzde yaygın olarak kullanılan PET/BT sistemlerinde, bir PET tarayıcı ile birlikte 16, 32, 64 veya daha fazla kesitli BT cihazının eklenmiş hali bulunmaktadır. Bu birleşik portala eklenen iş istasyonu ve yazılım programları sayesinde hem anatomik korelasyon hem de atenüasyon düzeltmesi yapılabilmektedir. Son zamanlarda geliştirilen cihazlarda koroner kalsiyum skoru, BT anjiyografi vb. işlemleri de yapabilen teşhis amaçlı BT tarayıcıları bulunmaktadır (12).
PET tarayıcılarında BT yerine MR tarayıcının eklenmesi ile PET/MR sistemleri geliştirilmiştir. PET/BT sistemindeki gibi iki modalitenin aynı gövdede birleştirilmesiyle veya simultane sistem olarak adlandırılan eş zamanlı görüntüleme yapabilen, son teknolojiye sahip, birbiri içinde yerleşik bir şekilde tasarlanmış cihazlar
mevcuttur (10). PET/MR sistemlerinde yüksek manyetik alandan dolayı PET cihazlarının konfigürasyonlarında bazı değişiklikler ve performans kısıtlılıkları olabilmektedir. Atenüasyon düzeltmesi her iki PET/MR cihaz türünde de PET/BT cihazlarındaki kadar iyi yapılamayabilir. Fakat MR görüntülemenin kardiyoloji alanında değerli veriler sunması sebebiyle bu yeni birleşik PET/MR modalitesinin de yeni ilgi çekici klinik sonuçlar çıkarma potansiyeli mevcuttur.
Miyokart PET Perfüzyon Görüntülemede Kullanılan Radyofarmasötikler (Tablo 1)
O-15 Su
O-15 su, metabolik olarak stabil olması, serbestçe yayılabilmesi ve ekstraksiyon fraksiyonu bire yakın olması (%100) nedeniyle miyokardiyal kan akımının non-invaziv in vivo ölçümü için referans kabul edilir (13). Yarı ömrünün 122 sn olması nedeniyle yalnızca bünyesinde siklotron bulunan merkezlerde kullanılabilir (7). O-15 su, N-15’in protonlarla ışınlanması veya doğal Nitrojen 14’ün döteronlarla ışınlanması ile üretilir. İkinci üretim yöntemi, hedef malzemenin hava olması nedeniyle ucuz olması, gerekli döteron enerjisinin sadece 3 MeV olması ve üretim için küçük, sınırlı koruma gerektiren özel siklotronların normalden daha az maliyetli olması nedeniyle diğer perfüzyon ajanlarına göre daha avantajlıdır. O-15 su’nun maksimum pozitron enerjisi 1,7 MeV olup ve N-13 amonyak’tan daha yüksek fakat Rb-82’den daha düşük; uzaysal rezolüsyonu da ikisi arasındadır (14).
O-15 su’nun serbestçe yayılabilir özellikte olması ve miyokart dokusunda tutulmaması nedeniyle perfüzyon defektlerini veya miyokardiyal canlılığını gösteren statik görüntüler elde edilemez. Mutlak perfüzyon değerlerinin elde edilebilmesi için kinetik modellemeye ihtiyaç vardır ve anlamlı perfüzyon görüntüleri ancak bu modellemenin voksel düzeyinde yapılmasıyla elde edilebilir. O-15 su’nun serbest yayılabilme özelliği, bir intrinsik kısmi hacim düzeltmesi olan perfüze olabilen doku fraksiyonu (PTF) kavramını ortaya çıkarmıştır. Diğer perfüzyon ajanları PET’in sınırlı uzaysal çözünürlüğü nedeniyle parsiyel volüm etkisine maruz kalmaktadır. Bu durum O-15 su’da görülmez ve diğer perfüzyon ajanlarından önemli bir farklılığıdır (15). Ayrıca PTF, doku canlılığının bir belirteci olduğu gösterilen perfüze edilebilir doku indeksini (PTI) tahmin etmek için kullanılabilir. Böylelikle iskemiyi enfarktüsten ayıran perfüzyon ve canlılık tek bir taramada değerlendirilebilir. O-15 su’nun kinetik analizinde, geliştirilen otomatik yazılım paketleri sayesinde dinamik kan akımı görüntülerinden PTF, kan hacmi, sol ventrikül hacmi ve ejeksiyon fraksiyonu hesaplanabilir.
O-15 su’nun kısa yarı ömürlü olması, dinlenme-stres protokolünün 30 dakika içinde tamamlanmasına imkan sağlar. 400 mega bekerel’lik (MBq) iki enjeksiyondan oluşan tipik bir protokolde maruz kalınan doz 0,8 miliSievert’tir (mSv) (1 mSv/GBq) (16).
Rb-82
Rb-82, kalitatif ve kantitatif miyokardiyal PET perfüzyon ajanı olarak uzun yıllardır yaygın bir şekilde kullanılmaktadır. Rb-82’nin yarı ömrü 75 saniye olup büyük oranda (%95,5) maksimum 3,15 MeV enerjiye sahip bir pozitronun emisyonu ile, %4,5 oranında elektron yakalama ve gama emisyonu ile bozunur (17). Bozunma sırasındaki pozitronların yüksek enerji aralığı, PET görüntülerinin N-13 ve F-18’e göre daha düşük intrinsik uzaysal çözünürlüğüne neden olur. Rb-82, potasyum (K) ile aynı biyolojik özelliklere sahiptir ve Na-K-ATPaz pompası yoluyla miyokart hücreleri tarafından tutulur. Rb-82 canlı miyokart hücrelerine alınırken, fibrotik dokudan hızla temizlenir. Ekstraksiyonu ilk geçiş sırasında yüksektir (%65) ancak artan kan akışıyla doğrusal olmayan bir şekilde azalır (18). KAH tespitinde Rb-82 PET, Talyum-201 ile SPECT kıyasla daha yüksek tanısal performans göstermiştir (19).
Rb-82, Stronsiyum-82 (Sr-82)/Rb-82 jeneratöründen üretilir. Bu jeneratörden elde edilen sağımda Sr-82 ve Sr-85 oluşma riski mevcuttur. Bu risk jeneratörün yaşı ve sayımın total hacimiyle artmakla birlikte yeni geliştirilen jeneratör sistemlerinde ikinci bir enjektör yardımıyla otomatik olarak kontrol altına alınmaya çalışılmıştır.
Rb-82’nin 3D modunda PET görüntüleme için hastalara verilecek önerilen dozu 10 MBq/kg’dır (minimum doz 740 MBq ve maksimum doz 1480 MBq). 2D modunda PET için bu enjekte edilen aktivitelerin iki katına çıkarılması gerektiğinden, 3D modunda PET görüntüleme önerilmektedir (20). Maruz kalınan radyasyon dozu kullanılan protokole bağlı olmakla birlikte 10 MBq/kg’lık iki enjeksiyonda yaklaşık 1,5 mSv’dir (16).
Rb-82, PET miyokardiyal perfüzyon görüntüleme için oldukça uygundur. Jeneratörden elde edilmesi, kısa yarılanma ömrü sayesinde miyokartta rezidüel aktivite kalmadan 30 dakika içinde istirahat ve stres PET görüntülemelerinin yapılabilmesi ve miyokardiyal canlılık ve kontraktilitenin değerlendirilmesine imkan tanıması önemli avantajlarıdır. Bununla birlikte yayılan pozitronun yüksek enerjisi nedeniyle uzaysal çözünürlük ve görüntü kalitesinin kötüleşmesi ve miyokardiyal dokudaki tutulumunun kan akışı ile doğrusal olmaması nedeniyle kantitasyonun etkilenmesi dezavantajlarıdır.
N-13 Amonyak
N-13 amonyak, uzun yıllardır miyokardiyal kan akımı çalışmalarında kullanılmaktadır. Bir siklotron ürünüdür ve O-16 (p,a) N-13 nükleer reaksiyonu yolu ile elde edilir. Nispeten düşük bir pozitron enerjisine (1,19 MeV) ve 9,96 dakikalık bir yarı ömre sahiptir (6). N-13, kanda temelde amonyum iyonu şeklinde bulunsa da indirgenerek amonyağa dönüştürülür. N-13 amonyak lipofilik özelliğinden dolayı hücre membranından pasif difüzyonla geçiş gösterdiğinden ilk geçiş ekstraksiyon fraksiyonu oldukça yüksektir (>%80). Miyokart hücresi içinde ya N-13 glutamin sentezine katılır (metabolik yol) ya da vasküler alana geri difüze olur. Miyokardiyal tutulumu, kan akımı artışı, ekstraksiyon fraksiyonu ve metabolik durum gibi çeşitli değişkenlerden etkilenir. N-13’ün ekstraksiyonu kan akışıyla ters ve doğrusal olmayan bir şekilde ilişkili olup metabolik durum daha az etkilidir (21). Elektrokardiyografi (EKG)-gated PET çalışmaları yüksek kalitededir ancak stres görüntüleme çalışması N-13’ün enjeksiyonundan sonra biraz gecikmeli yapıldığından dolayı stres anındaki gerçek fonsiyonel durumu tam olarak yansıtamayabilir.
N-13, yüksek ekstraksiyon fraksiyonu, uzun yarı ömrüve düşük pozitron enerjisi nedeniyle miyokardiyal kan akışının mutlak kantitatif ölçümü için oldukça değerlidir, diğer perfüzyon ajanlarına göre daha yüksek kaliteli görüntüler elde edilmesine imkan sağlar. Fakat bir istirahat-stres çalışması süresi diğerlerine göre hafifçe daha uzundur (yaklaşık 1 saat). 400 MBq’lik iki enjeksiyondan oluşan tipik bir protokolde, 1,8 mSv’den daha düşük bir doz maruziyeti bulunmaktadır.
F-18 Flurpiridaz
F-18 Flurpiridaz, elektron taşıma zincirindeki mitokondrial kompleks (MC)-1’in bilinen bir inhibitörü olan piridabenin yapısal bir türevidir. Deneysel çalışmalarda, F18-flurpiridaz’ın miyokardiyal dokudan hızlı bir şekilde alınması fakat yavaşça temizlenmesi oldukça uygun kinetik özellikler sağlamaktadır (22). Sonuç olarak, miyokardiyal tutulumu diğer perfüzyon ajanlarıyla karşılaştırıldığında gerçek mutlak miyokardiyal kan akımına oldukça yakındır ve bu da yüksek akış hızlarında kan akımı ölçümünde değişkenliğini azaltır. Daha da önemlisi, kan akımından bağımsız yüksek miyokardiyal ekstraksiyon oranı (ilk geçiş ekstraksiyonu >%90), minimum akciğer tutulumu ve hızlı hepatik klirens özelliklerine sahiptir ve çok iyi düzeyde kalp-akciğer (14,1) ve kalp-karaciğer (8,3) oranları göstermektedir (23).
Diğer miyokart PET perfüzyon ajanlarına göre uzun yarı ömürlü olması (110 dk) nedeniyle hemen yakınında siklotron bulundurulması gerekmez, bu önemli bir avantajıdır. Düşük pozitron menziline (<1 mm) sahip olduğu için hem daha yüksek kalitede görüntüler elde edilir hem de radyasyon maruziyeti düşüktür. Ayrıca fiziksel egzersiz ile miyokart görüntüleme protokollerinde olduğu gibi geç görüntüleme yapılabilmesi miyokardiyal canlılık değerlendirilmesine de imkan sağlar (23).
Miyokart PET Perfüzyon Görüntüleme Protokolleri
Stres Protokolü
Kantitatif miyokardiyal kan akımı ölçümünde kantitatif değerlendirmenin dinamik fazda yapılması gerektiğinden farmakolojik stres mümkün olan tek seçenektir. Stres protokolleri genellikle tüm perfüzyon ajanları için benzerdir ve SPECT miyokart perfüzyon görüntüleme ile aynıdır (20,24). Yaygın olarak kullanılan stres ajanları dipiridamol, adenozin ve son zamanlarda regadenozondur. Ancak dipiridamol birçok Avrupa ülkesinde bu endikasyon için onaylanmamıştır ve artık tavsiye edilmemektedir. Yaygın olarak kullanılan vazodilatörler, özellikle astım bileşenlerinin eşlik ettiği şiddetli kronik obstrüktif akciğer hastalığı durumunda kontrendike olabilir. Alternatif bir stres testi, atropin ile kombine edilmiş dobutamin olabilir, ancak maksimum kan akımına ulaşılıp ulaşılamadığı hala tartışılmaktadır.
Hastaların en az 6 saat aç kalmaları ve en az 12 saat kafeinli içecek, yiyecek ve kafein içeren analjeziklerden, 48 saat ise ksantin içeren ilaçlardan uzak durmaları gerekmektedir. Dipiridamol/persantin, vazodilatör infüzyonundan 24 saat önce kullanımı bırakılmalıdır.
İskemik EKG değişikliklerini ve potansiyel indüklenen aritmileri belirlemek için stres sırasında arteriyel kan basıncının izlenmesi ve 12 derivasyonlu EKG kaydı yapılması önerilir. Hastalara, semptom varlığı durumunda bile rahat olmaları ve hareketten kaçınmaları gerektiği konusunda ayrıntılı bir şekilde bilgi verilmesi tavsiye edilir. Regadenozonun yarı ömrü adenozinden daha uzundur ve daha tolere edilebilir yan etki profili nedeniyle, hastanın hareket etme olasılığını azaltarak, stres çalışmasını önemli ölçüde kolaylaştıracağı için en avantajlı seçenek olarak görünmektedir. Ek olarak, dipiridamol ile karşılaştırıldığında benzer stres miyokardiyal kan akımı değerleri rapor edilmiştir (25).
En iyi hasta pozisyonu sırt üstü, kolların başın üzerinde olduğu pozisyondur. Bu pozisyonun nispeten uzun bir süre korunması gerektiğinden, hastanın rahat etmesi ve gereksiz çaba harcamadan hareketsiz kalabilmesi için mümkün olan tüm özen gösterilmelidir. Kol dayanakları veya diğer destekleyici önlemler bu amaç için faydalı olabilir.
Görüntüleme Protokolleri
PET/BT sistemlerinin çoğunda, atenüasyon düzeltmesi için BT görüntüleme, PET görüntülemeden önce yapılır. BT görüntüleme sırasında hastalara düzenli nefes almaları, PET görüntülemeye geçiş ve görüntüleme sırasında hareketten kaçınmaları söylenmelidir. Solunum gatingi eşliğinde düşük doz BT, PET görüntülerine en yakın eşleşmeli bir atenüasyon haritası sağlar, fakat tüm solunum döngüsünü kapsadığında yüksek radyasyon dozu kaçınılmaz olur. Bu nedenle düzenli serbest nefes alınan nispeten yavaş bir BT görüntüleme ikinci en iyi seçenektir. Düşük doz BT ile alınan radyasyon dozu <1 mSv, en son nesil ultra düşük doz BT olan PET/BT tarayıcılarda ise 0,1 mSv’tir (26).
Miyokardiyal perfüzyon PET görüntülemenin standart protokolü istirahat-stres şeklindedir. Her iki çalışma aynı seansta gerçekleştirildiğinden, stres farmasötik ajanının istirahat perfüzyon çalışması üzerindeki olası kalıntı etkilerinden kaçınılmış olur. Kullanılan radyofarmasötiğin yarı ömrüne ve kinetik özelliklerine göre protokol tercihi yapılabilir (Şekil 1).
O-15 Su
Miyokartla sınırlı kalan diğer perfüzyon ajanlarının aksine O-15 serbestçe difüze olur. Bu nedenle çekim protokolleri tam bir kantitasyon sağlamak için arteriyal girdi fonksiyonu elde etme üzerine odaklanmıştır. Stres görüntülemede O-15 su, maksimum vazodilatasyon elde edildikten sonra bolus enjeksiyon şeklinde uygulanır. Ardından ikinci bir intravenöz yoldan serum fizyolojik ile yıkama yapılır. Tercihen uygulama, sabit bir bolus sağlamak için hız kontrollü otomatik bir enjeksiyonsistemi kullanılarak yapılmalıdır. Örneğin 5 mL O-15 su 1 mL/s, takiben 35 mL serum fizyolojik 2 mL/s şeklinde ayarlanabilir. O-15 su enjeksiyonuyla birlikte dört dakikalık bir süre boyunca dinamik görüntüleme başlatılır; bu süre, kan ve doku arasındaki dengeye daha öncesinden ulaşıldığı için yeterlidir (15). Adenozin infüzyonunun tüm stres taraması boyunca sürdürülmesi önemlidir. Adenozinin biyolojik yarı ömrünün nispeten kısa olması, dört dakikadan daha uzun süreli tarama yapılamamasının başka bir nedenidir. Radyofarmasötik uygulaması yapan kişi ile görüntüleme odasındaki teknisyen arasında iyi bir iletişimin olması önemlidir. Stres görüntüleme, O-15 su’nun kısa fiziksel yarılanma ömrü göz önüne alındığında, istirahat görüntülemeden 10 dakika kadar kısa bir süre sonra elde edilebilir. Atenüasyon düzeltmesi için kalbin stres anındaki hareketi (myokardiyal creep) gözönünde bulundurulduğunda solunum gated düşük doz BT, ideal olarak istirahat ve stres için ayrı ayrı elde edilir. Şunu vurgulamak gerekir ki perfüzyon miktarının kantitatif belirlenmesi O-15 su’nun alım oranından ziyade temizlenme oranına dayanmaktadır. Atenüasyon düzeltmesi zaman-aktivite eğrilerinin genliğini etkileyip şeklini pek fazla değiştirmediğinden, hatalı bir atenüasyon düzeltmesi miyokardiyal kan akımı değerlerini çok etkilemez. O-15 su ile yapılan atenüasyon düzeltmesiz çalışmaların, miyokardiyal kan akımı değerleri üzerine çok az etkili olduğu gösterilmiştir (15).
Rb-82
Rb-82 ile görüntüleme çalışması genellikle stres ile meydana gelen etkileri (iskemi sonrası miyokardiyal sersemleme) azaltmak için istirahat görüntüleri ile başlar. PET görüntülerinin atenüasyon düzeltmesi için; istirahat çalışmasından önce, stres çalışmasından sonra düşük doz BT görüntüleri elde edilmelidir. Stres çalışması sonrası alınan BT görüntülerinin, radyasyon dozunu azaltmak amacıyla hem istirahat hem de stres çalışmalarının atenüasyon düzeltmesi için kullanılması önerilebilir fakat kalbin hareketine bağlı olası etkiler de düşünülmelidir.
Jeneratörün tamamen yenilenebilmesi için istirahat ve stres enjeksiyonları arasında minimum 10 dakikalık bir süre gereklidir. Hem istirahat hem de stres PET çekimleri için aynı protokol izlenir. PET verileri en az 5 dakika boyunca, miyokardiyal kan akımı (MKA) hesaplamaları için gated ve dinamik veri kümelerinin yeniden gruplanmasına izin veren liste modunda alınır. Sr-82/Rb-82 jeneratöründe sağımı başlatmak için düğmeye basıldığında, PET sisteminde görüntüleme işlemi de başlatılmaya hazır olmalıdır. Daha sonra PET dedektörlerinde aktivite tespit edildiği anda dinamik görüntüleme başlatılır (17).
N-13 Amonyak
N-13 Amonyak ile yapılan istirahat ve stres çalışmaları arasında en az 5 yarılanma ömrü (en az 30 dakika) bırakılmalıdır. Kısaltılmış protokoller istirahat halinde enjekte edilen dozun rezidüel aktivitesine göre ayarlama yapılmasını önermiştir, ancak düzeltme yöntemlerinin etkinliği henüz kesin olarak belirlenememiştir. Stres çalışması için hastaların muayene yatağında yeniden konumlandırılması gerektiğinden, atenüasyon için genellikle ikinci bir BT görüntüleme gerekir. Enjeksiyon ideal olarak otomatik bir enjeksiyon sistemi kullanılarak yapılmalıdır ve görüntü işlemi, enjeksiyonunun başlamasından hemen veya birkaç saniye önce başlatılmalıdır. Optimum görüntüleme protokolü, yaklaşık 10 dakika boyunca liste modunda olmalıdır. Veriler daha sonra MKA ölçümü için gerekli dinamik görüntü dizisini ve görsel değerlendirme ve hacim hesaplamaları için gated görüntülerini elde etmek üzere yeniden gruplandırılır. Alternatif olarak kantitatif MKA ölçümü için 10 dakikalık bir liste modu veya çerçeve modunda görüntüleme ve ardından 5-10 dakikalık statik istirahat ve stres gated görüntüleme yapılabilir (21).
Görüntü Rekonstrüksiyonu
Tüm Perfüzyon Ajanları İçin Ortak Öneriler
Görüntüleme sırasında elde edilen veriler geometri, rastlantısallık, saçılım, normalizasyon ve ölü zaman kayıpları açısından düzeltilir. Genel öneri 2-3 mm’lik bir piksel boyutunun kullanılmasıdır, ancak kantitasyonu etkilemeyen biraz daha büyük boyutlar da kullanılabilir. İteratif rekonstrüksiyon yöntemleri günümüzde 3D görüntüleme gerçekleştiren çoğu tarayıcıda standart olarak kullanılmaktadır. Genel olarak bu algoritmalar, standart filtreli geri projeksiyon yöntemi ile karşılaştırıldığında hem görüntü kalitesini hem de sinyal/gürültü oranını iyileştirir, ancak tarayıcının özelliklerine de bağlı olarak mümkün olan en iyi yöntem konusunda hala belirsizlikler vardır (27). Ayrıca, rekonstrüksiyon algoritmasının tipinin değiştirilmesinin MKA ölçümünü etkileyebileceği de dikkate alınmalıdır.
Atenüasyon Düzeltmesi
Atenüasyon düzeltmesi için kullanılan BT gibi yüksek çözünürlüklü görüntüler ile birden fazla kalp döngüsü ve solunum fazını içeren bulanık PET görüntüleri arasındaki tam örtüşememe durumu, kardiyak PET için temel bir sorun olmaya devam etmektedir. Tercihen, solunum gated için kullanılana benzer bir protokol olan solunuma duyarlı düşük dozlu BT kullanılmalıdır. Bu seçenek mümkün değilse, düzenli yüzeysel nefes alma, en etkili şekilde üst üste binebilecek bir BT ve PET görüntüsü elde etmek için tercih edilen koşuldur. Bununla birlikte, görüntüler PET ve BT arasındaki doğru hizalama açısından her zaman kontrol edilmeli ve yanlış hizalama, rekonstrüksiyon öncesinde düzeltilmelidir. Metal artefaktlar, rekonstrüksiyon algoritmaları için zorluk teşkil edebilir ve doğru atenüasyon haritaları üretmek için bunların ekarte edilmesi gerekir. Şu anda, modern BT sistemlerinde çeşitli metal artefakt azaltma yöntemleri uygulamaya konmuştur (26).
Solunum ve Hasta Hareketi Düzeltmesi
Solunumun ve hasta hareketinin kardiyak görüntüler üzerindeki olumsuz etkisi açık bir şekilde gösterilmiştir. Rekonstrüksiyon algoritmasında, solunum ve hasta hareketi artefaktlarının düzeltilmesi için, solunum hareketinin bir karın kemeri ile sınırlandırılması da dahil olmak üzere çeşitli yaklaşımlar önerilmiştir (28). Bununla birlikte oldukça karmaşık olan bu yöntemlerin hiçbiri yaygın olarak uygulanmamaktadır.
Dinamik Görüntüler
Radyoaktivitenin kalpten ilk geçişi sırasındaki görüntü karesi (frame) süresi genellikle 5 saniyeden az değildir. Daha sonra görüntü karesi süresi kademeli olarak artırılabilir. MKA ölçümünün gerçekleştirileceği dinamik görüntülerin dizisi, olası hareket artefaktları açısından kontrol edilmelidir. Kantitatif ölçümler üzerine etkisi büyük olan, zaman aktivite eğrilerini elde etmek için gereken hızlı görüntü alımı sırasındaki görüntü kareleri arası hareket oldukça önemlidir ve düzeltilmesi zordur. Nispeten sınırlı solunum veya hasta hareketi bile sol ventrikülün ve miyokart duvarının konumunu etkileyebilir. Bazı yazılım paketleri, hareket düzeltme özelliğine sahiptir. Eğer bu mümkün değilse tek tek bazı framelerin silinmesi düşünülebilir (20).
Her Bir Radyofarmasötik İçin Özel Öneriler
O-15 su
O-15 su ile statik görüntüleme yapılamaz ancak gated görüntüleme ile hacimler ve EF, ilk geçiş kan hacmi görüntüleri kullanılarak tespit edilebilir. Bunun için, verilerin liste modunda alınması gerekir. Böylece hem dinamik hem de gated görüntüler (enjeksiyon hızına bağlı olarak enjeksiyondan yaklaşık 10-50 saniye boyunca) yeniden oluşturulabilir. Görsel olarak yorumlanabilir durumdaki görüntüler, dokudan kan hacminin dijital olarak çıkarılması teknikleri yanı sıra miyokardiyal kan akımının voksel düzeyinde otomatik parametrik görüntüleri kullanılarak oluşturulabilir fakat 3D perfüzyon görüntülerinden hesaplanması tercih edilmektedir ve bunu yapabilen yazılım programları ticari olarak temin edilebilmektedir (15). Bu programlar rutin olarak 3D perfüzyon görüntülerinden Amerika Kalp Topluluğu (American Heart Association, AHA) standart 17 segmentli modeline göre bölgesel MKA ve bölgesel miyokardiyal akım rezervini (MAR, yani stres ve istirahat MKA oranı) göstermektedirler (29). Büyük ölçekli klinik çalışmalarda doğrulanmış olmasına rağmen, O-15 su için tıbbi uygulamada kullanımında henüz The Food and Drug Administration (FDA) onayı yoktur, ancak birçok Avrupa ülkesinde onaylanmıştır.
Rb-82
Rb-82 ile görüntüleme işleminin sonunda, kalbin PET ve BT çekimlerindeki konumu, özel yazılım kullanılarak atenüasyon düzeltmesi için görsel olarak eşleştirilir. Liste modunda görüntü elde edinimlerinden, hem istirahat hem de stres çalışmaları için üç farklı PET rekonstrüksiyon veri seti elde edilebilir: Statik (non-gated) görüntüler, enjeksiyondan sonra 90-120 saniye ve 5-8 dakika arasında, kandaki sinyal düştüğünde elde edilen; enjeksiyondan sonra aynı zaman aralığında elde edilen PET verilerinin yeniden yapılanması ile oluşturulan görüntüler; genellikle 8’e (gürültü azaltmak için en iyi seçim) veya 16’ya (daha iyi eğri elde edilen) bölünen gated görüntüleri ve dinamik PET görüntüleridir. Dinamik PET edinimi için çeşitli zaman çerçevesi şemaları önerilmiştir. Sol ventrikül ejeksiyon fraksiyonu (SVEF) <%30 olan hastalarda, statik ve gated çekimlerin yeniden yapılandırılması işlemine, rezidüel kan sinyali düzeyini azaltmak ve miyokart ile sol ventrikül (SV) boşluğu arasındaki kontrastı iyileştirmek için enjeksiyondan 150-180 saniye sonra
başlanmalıdır (17).
N-13 Amonyak
N-13 amonyak için liste modu veri elde edilmesi şu anda tercih edilen yöntemdir. Mutlak kantitasyon için dinamik görüntüleme, giriş işlevi ve radyofarmasötik alım aşamaları için kısa süreli framelerle başlayarak (ilk 2-3 dakika) ardından 30 saniyelik veya 1 dakikalık artan süreli framelerle devam eden veri elde edilmesi şeklinde yapılır. Gated görüntüleme 8 bölmeli veya 16 bölmeli olarak elde edilebilir (21).
Miyokardiyal Perfüzyon PET Görüntülerinin Yorumlanması
Perfüzyon Görüntüleri (Rb-82 ve N-13 Amonyak)
Elde edilen görüntülerin, atenüasyon düzeltmesi ve rekonstrüksiyonu sonrası miyokart perfüzyon görüntülemede olduğu kalp eksenine göre yeniden düzenlenmesi gerekmektedir. Halihazırda çoğu cihazda, SPECT miyokart perfüzyon görüntüleme için kullanılan yazılım programlarının aynısı bulunmaktadır. Perfüzyon görüntülerini işlemlerken fizyolojik tutulum yerlerini ve görüntü kalitesini kontrol etmek önemlidir. Verilerin normalizasyonu ve üç eksende (kısa eksen, dikey eksen ve yatay uzun eksen) yan yana görselleştirilmesi yapılır. Kantitatif miyokardiyal PET çalışmasında, radyofarmasötiğin miyokardiyal tutulumunun kalitatif açıdan da yorumlanması ve raporlanması gereklidir. Mevcut yazılım programlarının çoğu miyokardiyal tutulumun polar harita görüntülerini sunmakta ve bireysel hasta sonuçlarının bir referans veritabanıyla karşılaştırılmasına olanak sağlamaktadır (veya kullanıcının kendi normal veri tabanını oluşturmasına olanak sağlamaktadır). Bu nedenle miyokardiyal kan akımının kantitatif ölçümünü, radyofarmasötiğin dağılım durumuyla entegre etmek ve normal referans değerler ile karşılaştırmak mümkündür ve yapılması tavsiye edilmektedir. Görsel-yarı kantitatif görüntü analizi, 17 segment (AHA modeli) kullanılarak bölgesel bazda gerçekleştirilir ve her bir segment, 0 (normal perfüzyon), 1 (hafif derecede azalmış perfüzyon), 2 (orta derecede azalmış perfüzyon), 3 (ciddi derecede azalmış perfüzyon), 4 (perfüzyon yok) arasında değişen 5 puanlık bir ölçek kullanılarak derecelendirilir. Bu derecelendirme, hem stres hem de istirahat miyokardiyal perfüzyon görüntüleri için toplam bir perfüzyon puanı sağlar. Anormal PET miyokardiyal perfüzyonu normal PET miyokardiyal perfüzyonundan ayırmak için belirlenen eşik değerleri çeşitlilik göstermektedir. En yaygın kabul gören eşik değer, toplam stres puanının (SSS) dikkate alınmasıdır ve ≥4 anormal olarak değerlendirilmiştir (30). Ancak daha kısıtlayıcı eşik değerler de önerilmiştir. Örneğin, Hsiao ve ark. (31) SSS >0’ı anormal olarak sınıflandırmıştır. Benzer şekilde Dorbala ve ark. (32) puanların yüzdelik ifadelere dönüştürülmesini ve %SSS >%1’in anormal olarak değerlendirilmesini önermiştir. Resim 1’de mikrovasküler hastalık lehine yorunlanan bir N-13 amonyak PET miyokart perfüzyon çalışması görülmektedir.
Gated Çalışmaları
Çoğu yazılım programı, hem gated görüntüleri hem de toplam statik görüntüleri aynı anda işlemler ve analiz eder. SPECT miyokart perfüzyon görüntüleme için kullanılan programlar genellikle gated PET çalışmalarında da kullanılır. Gated çalışmalarla SV hacimleri ve SVEF hesaplanabilir ve senkronizasyonu değerlendirilebilir. Gated çalışmaların bir sine döngü fonksiyonu kullanılarak görsel olarak görüntülenmesi, bölgesel SV duvar hareketinin değerlendirilmesine olanak tanır. Sol ventrikül diyastol sonu ve sistol sonu perfüzyon polar haritaları ile birlikte duvar hareketi ve kalınlaşmasının da polar haritaları elde edilebilir (33). Yukarıda belirtildiği gibi, Gated PET’te fonksiyon değerlendirmesini yapan programlar, Gated SPECT için halihazırda yaygın olarak kullanılan ve doğrulanan programlardan farklı olmadığından, ayrı bir normallik değeri belirlenmemiştir. Ancak çeşitli yazılım paketleri arasında farklılıklar rapor edilmiştir. İstirahat ve stres gated görüntülerin yan yana görüntülenmesi, SV duvar hareketi ve global fonksiyondaki değişiklikleri tanımlamak için faydalıdır. SVEF değişikliğinin değerlendirilmesi (yani istirahat ve stres çalışmaları arasındaki SVEF’deki değişiklik) ile ilgili olarak, <%5 birim değişikliğin şiddetli KAH’yi dışlamak için çok yüksek bir tahmin değerine sahip olduğu ve buna karşılık, >%5 birim değişikliğin, şiddetli KAH için çok yüksek bir pozitif öngörü değerine sahip olduğu belirtilmiştir (34). N-13 amonyak protokolünde, Rb-82’ye göre stres ve gated PET görüntüleme arasında hafifçe daha uzun bir süre olduğu ve daha doğru sonuç verdiği göz önünde bulundurulmalıdır. Diğer yandan gated SPECT çalışmalarına göre zaman aralığı yine de çok kısadır fakatN-13 amonyak ile sol ventrikül fonksiyonları üzerinde stresle indüklenen değişikliklerin gösterilebileceğini öne süren çalışmalar vardır (35).
O-15 Su İçin Özel Öneriler
Daha önce bildirildiği gibi, O-15 su perfüzyon PET, iyi bir kantitasyon sağlar ve akım değerlerinin derecelendirilmesinin, görsel perfüzyon derecelendirilmesinin tanısal doğruluğundan daha iyi performans gösterir. Bu nedenle, O-15 su PET’in geleneksel toplam stres puanı (SSS), toplam istirahat puanı (SRS) ve toplam fark puanı (SDS) terimleriyle ifade edilmesi nadir bir durumdur. Parametrik görüntüler iskemik alanı ve yaygınlığını görsel olarak tanımlamak için kullanılmaktadır; MKA ve MAR’ınbelirlenen eşik değerleri de normal ve anormal perfüzyonu ayırmak için kullanılmaktadır. En çok kullanılan yaklaşım, yakın zamanda PACIFIC çalışmasında da doğrulanan eşik değere dayanmaktadır ve kan akımının 2,30 mL/dakika/gram veya daha az olduğu en az iki bitişik miyokart segmentinin varlığı bulgusunu anormal olarak sınıflandırmaktadır. Radyofarmasötiğin tutulum görüntülerine dayanan gated PET’in standart değerlendirilmesi O-15 su için yapılamaz fakat SVEF, enjeksiyon sonrası ilk dakikalarda alınan gated ilk geçiş veya parametrik kan hacmi görüntüleri kullanılarak belirlenebilir (36).
Miyokardiyal Kan Akımının Ölçülmesi
Genel İlkeler
Miyokardiyal kan akımı kantitasyonu için kompartman modeli kulanılabilir. Tek kompartman modelinde k1 sabiti kandan dokuya gram doku başına mL cinsinden radyofarmasötik taşınma oranını, k2 sabiti ise dakikadaki temizlenme oranını gösterir. Bu basit modelleme, enjeksiyondan sonraki ilk dakikalarda hem O-15 su hem de Rb-82’nin kinetiğini tanımlayabilir. N-13 amonyağın kinetiğini doğru bir şekilde tanımlamak için, glutamin havuzuna difüzyonu tanımlayan k3 hız sabitini içeren ikinci bir kompartman eklenmelidir. Ancak analizi ilk dört dakikayla, dolayısıyla metabolik süreç başlamadan önceki zamana sınırlandırarak bu bölümün göz ardı edilmesi önerilmiştir (37). O-15 su için K1, miyokardiyal kan akımı ile aynıdır ve k2 de miyokardiyal kan akımı ile orantılıdır çünkü su serbestçe yayılabilir ve dokuya giren suyun kütle dengesini sağlamak için dokudan benzer bir miktarda temizlenmesi gereklidir (38). Kompartman modelini açıklayan denklem aşağıdaki gibidir:
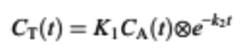
Burada, CA(t) tarama sırasında zaman içinde arteriyel kandaki radyoaktivite konsantrasyonudur, CT(T) zaman içinde dokudaki radyoaktivite konsantrasyonudur. Miyokardiyal duvardaki ilgi alanı hacmi (VOI) veya voksel içinde ölçülen radyoaktivite konsantrasyonu kandaki aktiviteyi ve kalp hareketi nedeniyle sol ve sağ ventriküler boşluklardan yayılan aktiviteleri de içerdiğinden ve PET’in sınırlı uzaysal çözünürlüğü de düşünüldüğünde, toplam PET sinyali [CPET(t)] şu şekilde tarif edilebilir:
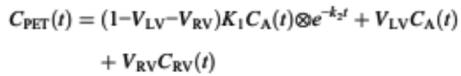
V =hacim fraksiyonu
O-15 Su
Miyokardiyal kan akımı kantitasyonu için tek kompartman modelini kullanan O-15 su PET, kinetik özellikleri sayesinde mükemmel bir kan akımı kantitasyonu sağlamakta ve referans standart olmaya devam etmektedir. Model, kısmi hacim düzeltmesinin yanı sıra sağ ventrikül (RV) ve SV kan havuzundan gelen radyoaktivitenin yayılma etkileri için de içsel bir düzeltme sağlar. PTF değerleri VOI veya voksel içindeki skar dokusu gibi perfüze edilemeyen dokuların neden olduğu, O-15 su’nun akımı ve temizlenme oranı arasındaki tutarsızlıklar için bir ölçü olarak görülebilir. Bu nedenle, O-15 su için MKA, transmural MKA’yı ölçen diğer PET radyofarmasötiklerinin aksine yalnızca perfüze edilebilir dokuda ölçülür. Transmural MKA daha sonra dolaylı olarak sol ventrikül hacmi (VSV) ve sağ ventrikül hacmi (VRV) de dahil edilip, MKA × PTF/(1 + VSV + VRV) formülü kullanılarak hesaplanabilir. PTF’nin anatomik doku fraksiyonuna (ATF) bölünmesi, miyokardiyal doku canlılığının bir belirteci olan PTI’nın (perfüze doku indeksi) hesaplanmasına olanak sağlar. PTI, modern bir PET/BT tarayıcısı kullanıldığında, kan hacmi görüntüsü denklemdeki VSV ve VRV’den elde edilir. Dolayısıyla O-15 su kullanılarak hem MKA hem de canlılık tek bir tarama kullanılarak değerlendirilebilir. O-15 şu ana kadar esas olarak seçili araştırma merkezlerinde kullanılmasına rağmen, klinik uygulamalarda kullanılan MKA ve MAR anomalileri için referans değerler tanımlanmıştır (39). Özellikle hiperemik MKA’nın KAH’yi tanımlamada kanıtlanmış etkinliği hibrit görüntüleme ve stres kantitatif PET çalışmaları için avantaj olmuştur.
Rb-82
Rb-82’nin kullanımı, miyokart perfüzyon görüntülemesi için PET’in yaygın olarak uygulanmasını mümkün kılmıştır. Yoshida ve ark. (40) radyofarmasötik enjeksiyonundan sonra iki dakikalık bir görüntünün elde edilmesine dayanan, retansiyon modeli olarak adlandırılan MKA kantitasyonu için basitleştirilmiş bir yaklaşım geliştirdiler. Son zamanlarda ise kompartman modelleri kullanılmaya başlanmıştır. Bu radyofarmasötiğin yaygın kullanımı nedeniyle hesaplanan değerlerin tekrarlanabilirliğine özellikle önem verilmiştir. Ancak normal deneklerde ölçülen değerler arasında farklılıklar vardır ve bu da farklı platformlar kullanılarak elde edilen verilerin karşılaştırılmasında biraz daha dikkatli olunmasını gerektirmektedir (20).
N-13 Amonyak
Miyokardiyal kan akımının kantitatif hesaplanmasında N-13 amonyak’ın retansiyonuna dayalı yaklaşımlar kullanılmış olmasına rağmen esas olarak kompartman modelleri tercih edilmektedir. Retansiyona dayalı yaklaşımda, miyokardiyal duvardaki sinyal, retansiyon hızı Ki ve N-13 amonyağın zaman içindeki plazma aktivitesinin integralinin, yani zaman içindeki değişim miktarının çarpımıyla ilişkilidir.
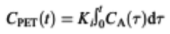
Her ne kadar Ki, miyokardiyal kan akışını K1’e göre daha az öngörse de, Şekil 2’deki kırmızı eğride görüldüğü gibi yine de miyokardiyal kan akımı ile orantılıdır. Önerilen kompartman modelleri, daha önce sözü edilen tek doku kompartman modeline benzeyen iki kompartmanlı model ve metabolizmayı hesaba katan üç kompartmanlı modeldir. İkinci modelde analiz, radyofarmasötik enjeksiyonundan sonraki ilk dört dakika ile sınırlandırılarak ve metabolik yol ihmal edilerek basitleştirilmiştir. Bu farklı kompartman modelleri ile elde edilen sonuçların birbiriyle yakından ilişkili olduğu kabul edilmiştir, ancak yine de önemli farklılıklar göstermektedirler. Son zamanlarda analizler kompartman modeli ve yazılım programlarının kombinasyonunu kapsayacak şekilde genişletilmiş ve MKA ölçümlerinde kısmen hasta özelliklerine de bağlı ortaya çıkan değişiklikler açısından bir uyum sağlanmaya çalışılmıştır (41).
Tuzaklar ve Artefaktlar
Genel Değerlendirme
Kantitatif PET’in ilk ve maalesef kaçınılmaz problemi, miyokart akım reservinin (MAR) değerlendirilmesinde dinamik egzersiz stres testi gibi fiziksel stres uygulanamamasıdır. Yukarıda bahsedildiği gibi, bu kısıtlama, enjeksiyon esnasında dinamik görüntüleme elde edilme gereksinimi ile ilgilidir ve daha uzun yarı ömürlü F-18 flurpiridaz gibi perfüzyon ajanları klinik kullanıma girse dahi engellenemeyecektir. F-18 flurpiridaz’ın standart tutulum değerine dayalı basitleştirilmiş bir yaklaşımın MAR’nin değerlendirilmesi için yeterli olup olmayacağı belirsizliğini korumaktadır (42). Ayrıca kantitatif PET’in olası bir diğer problemi de çekim esnasında hastaya sırtüstü yatan pozisyon verilme gereksinimidir.
Tüm kardiyak PET çalışmalarında problem olan atenüasyon düzeltmesi için gereken PET ve BT görüntülerinin hizalanması kantitatif çalışmalarda özellikle sorun olmaktadır (43). Ayrıca kantitatif çalışmalarda, çekim esnasında hareket artefarktı için tek kesit düzeltme yapmayı gerektiren işlemci yazılıma ihtiyaç duyulmaktadır (28,44). Bu konu muhtemelen kantitatif kardiyak PET için en büyük zorluktur. Özellikle farmakolojik stres nedeni ilegelişen kardiyak tırmanma (‘myocardial creep’) varlığında önlenmesi ve düzeltilmesi zor bir durumdur (45). Kantitatif PET’te diğer bir majör durum detektör yoğunluğu olmadan tek pik gösteren kaliteli enjeksiyon bolusudur (46). Çekimin geç başlatılması gibi olası karıştırıcı durumlar için zaman-aktivite eğrisi incelenmelidir. Miyokardiyal zaman-aktivite eğrisi geç fazında hasta hareketi anormal tepe olarak belirebilir (46). Girdi fonksiyonu ve miyokardiyal şekil çizimi yapmak için Rb-82 ve N-13 amonyak ajanlarının kullanımında genel problem geç tutulum görüntülerinden değerlendirmenin yapılıp sonrasında erken dinamik görüntülere transfer edilmesidir. Bu yaklaşım özellikle kardiyak tırmanma durumunda, çalışmanın erken ve geç fazlarındaki VOI’lerin farklı olabilmesi nedeni ile artefaktta sebep olmaktadır. O-15 su için tutulum görüntüleri yoktur ve O-15 su kardiyak tırmanma kaynaklı artefaktlara daha az duyarlı olduğu için VOI’nin dinamik verilerde tanımlanması gereklidir. Her durumda hasta hareketini efektif olarak tanımlamak için çekim esnasında VOI’nin kalp üzerindeki konumuna bakmak gerekmektedir.
Yukarıda bahsedilen muhtemel tuzaklardan bağımsız olarak, direkt olarak epikardiyal KAH’ın neden olduğu miyokardiyal iskemi anlamına gelmeyen anormal MKA piki veya daha sık olarak anormal MAR gibi kantitatif verilerin yorumu bazı durumlardan etkilenebilir. Özellikle, koroner bypass geçirmiş hastalarda greftler açık olmasına rağmen normal olmayan MKA görülebilir ve ancak işlemden aylar sonra normale dönebilir (47). Benzer olarak, sol ventrikül fonksiyon bozukluğu veya ağır böbrek hastalığında epikardiyal hastalığı olmadan ve normal perfüzyon bulguları ile normal olmayan değerler görülebilir (48). Tersine, daha önce miyokardiyal enfarktüs geçirmiş skar dokulu hastalarda pik MKA normal olmasına rağmen normal olmayan derecede düşük istirahat MKA nedeni ile yalancı normal MAR değeri saptanabilir. Tüm bu durumlarda, kantitatif PET veriler dikkatlice değerlendirilmelidir. Görüntü sayım dansitesi çalışmanın tanısal kalitesini ve güvenirliğini etkilemektedir. Vücut kitle indeksi, radyonüklit dozu, tarayıcı performansı, görüntüleme zamanı gibi ek faktörlerin PET görüntülerinin son sayım yoğunluğunu etkileyebileceği dikkate alınmalıdır.
O-15 su
O-15 su ile ilgili tuzaklar, enjeksiyon bolusu, PET rezolüsyonu, rölatif sayım hızı istatistiği, pozitronun orta derecede dağılımı, hasta hareketi ve yetersiz kan akımı ile ilgilidir. O-15 su için tutulum görüntüsü yoktur. O-15 su kardiyak tırmanma nedenli artefakta daha az duyarlı olduğu için, VOI dinamik veriler üzerinden tanımlanır. Tutulum görüntüsü yokluğuna ek olarak O-15 su analizinin başlıca limitasyonları yüksek kan akımı aktivitesi ve sağ ve sol ventrikülden dağılım için düzeltme gerektirmesidir (42). Bu düzeltme kinetik modelleme ile yapılmaktadır ve O-15 su verisi analiz edecek tüm sistemlere uygulanır. O-15 su için PET’te kullanılabilecek özel ticari kantitatif yazılım programı şu ana kadar üretilmemiştir, bu nedenle analiz için kurum içi kinetik model bilgisine gereksinim bulunmaktadır. Bununla beraber O-15 su ile SVEF ölçümü yapan bazı paket programlar vardır ancak şu anda bunlar geniş olarak kabul görmemiştir (49). O-15 su miyokardiyal perfüzyon görüntüleme birçok Avrupa ülkesinde onaylanmıştır ve geri ödeme kapsamındadır.
Rb-82
Rb-82’ye spesifik tuzaklar, ajanın ilk geçişi sırasındaki detektör yoğunluğu ve jeneratörün eskimesi nedeni ile volümdeki Rb-82 aktivitesinin azalması ve bu nedenle kan ilk geçiş eğrisinin düzleşmesidir. İlk tuzağa ilişkin olarak, detektör doygunluğu riski ile ilk geçiş fazı ve sonraki kesitlerde yeterli aktivite ihtiyacını iyi dengeleyecek, gelişmiş tarayıcıları hesaba katan, optimize edilmiş enjeksiyon protokolleri önerilmektedir (50). İkinci noktayı ele alırsak, sabit infüzyon hız kapasiteli yeni gelişen enjektörler günümüzde kullanılabilmektedir (51). Görüntü kalitesine etki eden Rb-82’ye özel bir diğer problem, %13 oranında meydana gelen gama emisyonun bozunma olayı ve özel düzeltme gerektirmesidir (52). Son olarak, yüksek enerjili Rb-82 pozitronlarının, PET ajanları içerisinde en uzun menzile sahip olduğu akılda tutulmalıdır (14,23). Yüksek akım değerinde düşük ekstraksiyon, stres esnasında normal perfüze ve hafif hipoperfüze miyokart ayırımını zorlaştırır (23). Kronik obstrüktif akciğer hastalığı (KOAH) olan ve SV disfonksiyonu olan hastalarda akciğerde normal olmayan tutulum görülebilir (53). Yüzde on düzeyinde hastada gastrik Rb-82 tutulumu ve saçılımı görülebilir, bu nedenle miyokardiyal perfüzyon görüntülemede inferior duvar analizi etkilenebilir (53). Proton pompa inhibitör tedavisinin Rb-82 gastrik tutulumun yoğunluğunu artırdığı görülmektedir (54). Ek olarak, obezite ve geniş mide volümü PET miyokardiyal perfüzyon görüntülemede gastrik sinyalde bir artış etkisine neden olmaktadır, bu nedenle Rb-82 PET miyokardiyal perfüzyon görüntüleme öncesi obez hastalarda uygun açlık önermek görüntü kalitesini artıracaktır (55).
N-13 Amonyak
N-13 amonyak genel PET miyokardiyal perfüzyon görüntüleme tuzaklarına ek olarak daha özgül sorunlara sahiptir. Özellikle, esas olarak normal sol ventrikül fonksiyonlu kişilerde yan (lateral) duvarda bölgesel olarak tutulumda rölatif azalma görülebilir (56). Birçok güncel çalışma solunum hareketinin neden olduğu atenüasyon artefarktının bu bulguda majör rol oynadığını göstermektedir (56). PET miyokardiyal perfüzyon görüntülemede apikal inceliğin genellikle N-13 amonyak ve TOF kamera ile daha belirgin izlendiği saptanmıştır (57). Rb-82 gibi, KOAH olan ve sol ventrikül disfonksiyonu olan hastalarda normal olmayan akciğer tutulumu görülebilir. Dahası, ağır sigara içicilerinde de artmış akciğer tutulumu görülmektedir (58). Diğer tüm perfüzyon ajanlarında olduğu gibi (PET ve SPECT) normal olmayan sağ ventrikül tutulumu hipertrofi veya KOAH nedeni ile izlenebilir. Eğer sağ ventrikül duvarında tutulum sadece stres altında izlenir ise, bu durum sol ventrikülün diffüz iskemili ağır KAH durumunda ajanın miyokartta rölatif düşük tutulumu nedenli olabilir. Kantitatif perfüzyon ölçümüne özel tuzaklar, dinamik görüntüleme esnasında hareket artefarktı ve atenüasyon düzeltmede emisyon ve BT görüntülerinin yanlış hizalanmasından kaynaklanabilir. Başka bir açıdan, rölatif düşük aktiviteli N-13 amonyak Rb-82 ile karşılaştırıldığında, kalpten ilk faz bolus enjeksiyon esnasında ölü zaman riski azalır, ve N-13 amonyak ile alınan tutulum görüntülerinin kaliteli olması, kantitatif görüntüleme için gerekli olan VOI tanımlanmasını kolaylaştırır. Daha uzun yarılanma zamanı olduğu için, N-13 amonyak protokolü daha çok zaman gerektirir. Birden çok hastaya istirahat görüntülemesi yapılıp sonra ilk hastaya dönülerek stres çalışmasının yapılması bu kısıtlılığın üstesinden gelinmesini sağlar. Ancak, bu yaklaşım hasta açısından iş-zaman oranını iyileştirse bile, dezavantaj olarak her hasta için cihazda iki ayrı zaman ayrılmasına ve hasta pozisyonu ve emisyon ve BT görüntülerinin eşleştirilmesinde sıkıntıya sebep olur. Bu nedenle, kalan aktivitenin düzeltilmesi ile kısaltılmış protokol önerilmektedir (59,60). Gated PET değerlendirmesi için stres çalışması protokolü dikkate alınmalıdır.
Klinik Kanıtlar
O-15 Su
O-15 su, miyokardiyal kan akımı ölçümü için karakteri nedeni ile ideal ajan olarak kabul edilsede, KAH tanısı için etraflıca valide edilmelidir. Çünkü erken dönemde görsel parametrik görüntülerin elde edilmesi zordur ve validasyon çalışmalarının büyük çoğunluğu sağlıklı kişiler ve KAH hastaları arasında hiperemik MKA ve MAR değerlerinin optimal eşik değeri üzerine
odaklanmıştır (61). İnvaziv koroner anjiyografi ve fraksiyonel akım rezervi (FAR) referans olarak kullanılarak hiperemik MKA 2,5 mL/dk/gr eşik değer olarak alındığında KAH tanısı koymada %92 doğruluk oranına sahip olduğu bulunmuştur (62). Ek olarak, KAH tanısında hiperemik MKA (1,86 mL/dk/gr eşik), MAR’ye (2,3 eşik, %74) göre daha çok doğruluk (%84) oranına sahiptir. Hiperemik MKA’nın üstünlüğü, hafifçe farklı eşik değerler ile yakın zamanda yapılan çalışmalarda ispatlanmıştır (63,64). Bu çalışmalarda, FAR ile tanımlanan obstrüktif KAH’yi tespit eden optimal eşik değerler, hiperemik MKA için 2,3 ve 2,4 mL/dk/gr arası ve MAR için 2,5 bulunmuştur. Hiperemik MKA’nın MAR’ye göre yüksek tanı doğruluğu tek stres protokolü yolunu açmaktadır. Ek olarak, PACIFIC çalışması O-15 su’nun SPECT miyokardiyal perfüzyon görüntüleme veya kardiyak BT anjiyografiye (KBTA) göre yüksek doğruluk oranına sahip olduğunu göstermektedir (65). Diğer PET perfüzyon ajanları ile bu tarz prospektif çalışmalar henüz yeterli olmadığı için birebir karşılaştırma şimdilik yapmak mümkün değildir. Ek olarak, bu sonuçların daha önce KAH hikayesi olmayan ve normal SVEF’si olan hastalardan elde edildiği akılda tutulmalıdır. Diğer hasta gruplarında PACIFIC II gibi çalışmalar devam etmektedir. Diğer PET perfüzyon ajanlarının yanında, O-15 su PET güçlü prognostik bilgiler içerir ve KBTA ile gösterilebilen anatomik olarak anormal koroner yapıların tanısına katkıda bulunmaktadır.
Rb-82
Anjiyografide >%50 koroner darlık saptama özgüllük ve duyarlılığı için karşılaştırma yapıldığında, SPECT ile %87 ve %73, Rb-82 PET miyokardiyal perfüzyon görüntüleme ile %91 ve %89 olarak saptanmıştır (66). Obstrüktif KAH tanısında Rb-82 ile miyokardiyal perfüzyon görüntüleme ve SPECT miyokardiyal perfüzyon görüntülemenin karşılaştırıldığı sistemik bir derleme ve meta-analizde, onbeş Rb-82 PET ve sekiz kardiyak SPECT çalışması dahil edilmiştir (67). Koroner anjiyografide obstrüktif KAH tanısında Rb-82 PET ile tanı özgüllüğü ve doğruluğu sırası ile %90 ve %88, buna karşılık Teknesyum (Tc)-99m işaretli ajanlar ile gated-EKG ve atenüasyon düzeltmeli SPECT görüntülemede tanı özgüllüğü ve doğruluğu sırası ile %85 ve %85 olarak bulunmuştur. Düşük prevalanslı KAH hastaları dışlandığında, Rb-82 ile miyokardiyal perfüzyon görüntülemede tanısal doğruluk SPECT miyokardiyal perfüzyon görüntülemeye göre daha yüksek (eğri altındaki alan 0,95 vs. 0,90; p<0,0001), özgüllükte ise SPECT miyokardiyal perfüzyon görüntülemeye göre belirgin düşüklük (%70) saptanmıştır (19,68,69). Ayrıca, Rb-82 miyokardiyal perfüzyon görüntüleme SPECT miyokardiyal perfüzyon görüntüleme sonuçlarından bağımsız olarak efektif prognostik risk değerlendirmesi imkanı tanımaktadır (70). Yakın zamanlı prospektif kadın ve obez hastalarda yapılan bir çalışmada Rb-82 miyokardiyal perfüzyon görüntüleme kadmiyum çinko tellerüd kamera ile alınan SPECT miyokardiyal perfüzyon görüntülemeye göre yüksek duyarlılık göstermiştir (%85 vs. %57, p<0,05) (71). Miyokardiyal perfüzyon görüntüleme değerlendirmesinde MKA kantifikasyonu özellikle dengeli iskemi hastalarında kinik olarak yararlıdır (72). Görsel olarak normal PET miyokardiyal perfüzyon görüntülemeli semptomatik hastalarda MKA’da bozulma kötü prognoz ile ilişkilidir (73). Global MAR >1,9 değeri, yüksek riskli KAH’yi %97 negatif prediktif değeri ile dışlar (74). Tersine, global MAR <1,5 ise çok damar hastalığı prevalansı yüksektir, global akış rezerv değeri 1,5 ve 2,0 arasında ise mikrovasküler hastalık ile örtüşerek orta riskli seviyesindedir (75). Miyokardiyal perfüzyon görüntüleme ile orta seviye ölüm riski olan hastalarda, değerlendirmeye MAR eklenmesi, tekrar sınıflandırma yapılmasına sebep olup, bu hasta grubunun %17’sinin yüksek risk ve %34’ünün düşük risk grubuna dahil edilmesini sağlamıştır. Rb-82 PET MAR değerinde azalmanın miyokardiyal iskemi yaygınlığında güçlü ve artan prognostik değere sahip olduğu gösterilmiştir (76). Bilinen veya şüpheli KAH olan hastalarda, çok merkezli gözlemsel bir PET miyokardiyal perfüzyon görüntüleme çalışmasında iskemi ve skar genişliğinin ve şiddetinin, kardiyak ölüm ve tüm ölüm nedenlerinin tahmininde geleneksel koroner risk faktörlerden daha iyi olduğu gösterilmiştir (77). Kardiyak SPECT’in aksine, Rb-82 PET’te görüntüler farmakolojik stres esnasında alınmaktadır. KAH olmayan olgularda SVEF’de farmakolojik adenozin stres ile artış saptanır, oysa koroner anjiyografide çok damar hastalığı olanlarda artış olmadığı veya SVEF’de düşüş bile olduğu görülebilir (34).
N-13 Amonyak
Görsel ve semi-kantitatif analizlere dayalı çalışmalar N-13 amonyak PET’in, miyokardiyal iskemi saptamada Tl-201 miyokardiyal perfüzyon görüntülemeye göre üstün olduğunu göstermiştir ve bu sonuçlar Tc-99m işaretli ajanlar kullanılarak da ispatlanmıştır (1,78). Kantitatif PET perfüzyon verilerini içeren sonraki çalışmalar, KAH tanısı koymada mükemmel tanısal performansa sahip olduğunu ve MKA ve MAR’nin görsel değerlendirmeye değer kattığı gözlenmiştir (79). Kantitatif N-13 amonyak PET ile yapılan çalışmalarda, yüksek risk profilli semptomatik olmayan olguları tespit etmede etkili olduğu ve risk faktörlerinin kontrolü ile MKA’da düzelme elde edildiği gösterilmiştir (80,81,82). Yakın zamanlı birçok çalışma çok damar KAH tanısına kantitatif N-13 amonyak PET’in katkıda bulunduğunu göstermiştir (83). Perfüzyon ve kantitatif verileri karşılaştırdığımızda, normal olmayan perfüzyonun prognostik değeri doğrulanmıştır. Bununla birlikte normal perfüzyon izlenen düşük MAR bulunan hastalarda da yüksek kardiyak olay riski saptanmıştır. Benzer şekilde, kronik KAH olan hastalarda, MAR’de azalmanın kardiyak ölüm riski açısından SVEF’den daha duyarlı bir belirteç olduğu bulunmuştur (84,85). N-13 amonyak PET için normal ve normal olmayan MKA ve MAR değerlerini ayırt etmede eşik değerleri için çeşitli çalışmalar yapılmıştır. Hiperemik MKA (eşik 1,52 mL/dk/gr) ve MAR (eşik 2,74) karşılaştırıldığında, MAR koroner stenoz tespitinde anlamlı tanısal üstünlüğe sahiptir (79). Sonraki çalışmalar, hiperemik MKA için eşik değer 1,85 mL/dk/gr ve MAR için eşik değer 2,0 olarak belirtmiştir. Ancak, son bir çalışmada, KAH tespitinde MKA, MAR’ye göre daha etkili bulunmuştur (86). Öte yandan, MAR için eşik 2,0 değeri sonradan doğrulanmıştır (87). Değişik kantitatif metodlar kullanılarak yapılan başka çalışmalarda, MAR eşik değeri daha düşük (1,4) bulunmuştur (88).
Klinik Endikasyonlar
KAH tanı ve prognozunda kantitatif miyokart PET perfüzyon görüntülemenin değeri geniş ölçüde kabul görmüştür. Ancak, tüm PET çalışmalarında olduğu gibi SPECT çalışmaları ile karşılaştırıldığında maliyet, üretim ve taşıma problemi, PET sistemlerinin daha çok onkolojik olgular için kullanılması, PET miyokardiyal perfüzyon görüntülemenin ise daha çok yarar sağlayacak özel hasta grubunda tercih edilmesi gerektiği vurgulanmaktadır.
Tanı
- Tanısal amaçla, kantitatif miyokart PET perfüzyon görüntülemenin kullanımının en geniş kabul edilen endikasyonu diffüz çok damar KAH şüphesi durumunda gözden kaçırılabilecek olan dengeli iskemidir.
- Kalp yetmezliği, aritmi ve kardiyomyopatili hastalarda iskemi araştırılmasında kullanılabilir.
- Genellikle, kantitatif PET’in değer kattığı klinik durumlar, bilinen KAH olan, hastalığın daha derin patofizyolojik nedenlerinin anlaşılması gereken olgular veya karmaşık çok damar hastalığı şüphesidir (89,90).
- Kantitatif PET, semptomları miyokardiyal iskemi ile uyumlu olup, koroner anjiyografide anlamlı lezyon olmayan durumlarda da mikrovasküler hastalığı tespit edebilmektedir. Bu özellikle kadın hastalarda daha çok görülmektedir (91,92).
- Kardiyak BT anjiyografinin kullanımının artması ile, iskeminin varlığının belirlenmesi gereken, arada kalınan lezyonu olan çok sayıda hasta ortaya çıkmaktadır. Bu hastalarda iskemi değerlendirmesinde de kantitatif miyokart PET perfüzyon görüntüleme kullanılabilmektedir.
- Yüksek enerjili fotonlar, yüksek sinyalli ajanlar ve PET için uygun atenüasyon düzeltme tekniklerinin gelişmesi ile vücut kitle endeksi yüksek ve göğüs deformitesine sahip hastalarda PET kullanımı diğer bir endikasyon haline gelmektedir (93).
- Kalp transplantasyonu sonrası hem perfüzyon değerlendirmesi hem de yaygın nakil vaskülopatisini belirlemede kullanılabilir.
- Sarkoidoz şüphesi ile gelen hastalarda, metabolizma ve perfüzyonun doğru değerlendirilebilmesi amacıyla önerilmektedir.
- Daha tercih edilebilir bir dozimetre profili nedeniyle PET, özellikle genç yaşta ve konjenital kalp hastalığı olanlarda tercih edilmelidir.
Prognoz
Yapılan çeşitli çalışmalar, risk değerlendirmede MKA ve MAR kantifikasyonunun değerli olduğunu göstermektedir (93). Bölgesel tutulum bozukluğu genişliği, pik MKA, MAR ve SVEF rezervi gibi birkaç önemli prognostik parametreyi bir arada sunması nedeni ile kantitatif PET, KAH hastalarında risk değerlendirme aracı olarak oldukça önemli hale gelmiştir. Ancak, yukarıda bahsedilen ulaşım ve ekonomik sınırlandırmalar nedeni ile göğüs ağrılı hastalarda Gated SPECT miyokadiyal perfüzyon görüntülemenin de benzer risk sınıflamasını yapabildiği düşünüldüğünde kantitatif PET tercih edilmeyebilmektedir.
- Koroner dolaşımı etkileyen kardiyomiyopatiler ve en önemlisi hipertrofik kardiomiyopatilerde kantitatif PET mikrovasküler hastalık risk sınıflamasında en etkin yöntemdir (94,95).
- Kantitatif PET, diyabetik hastalarda, son dönem böbrek yetmezliğinde, mikrovasküler hastalık nedeni ile göğüs ağrılı fakat normal koroner arterli hastalar gibi yüksek riskli grupta prognostik sınıflamaya katkıda bulunmaktadır (96,97,98).
- Kalp nakli yapılmış hastalarda vaskülopati tanısında kantitatif PET en etkili yoldur (99).
Tedavi Değerlendirme
- Koroner rezervdeki rölatif azalmayı atlamadan, birçok ciddi darlık ve diğer lezyonları ayırt edebilmesi nedeni ile, kantitatif perfüzyon PET özellikle kompleks KAH hastalarına yaklaşımda gerekli bir yöntemdir (100,101).
- Kantitatif PET verilerinin asemptomatik KAH ve bu olguların risk faktörlerinin ve tedavi sonuçlarının değerlendirilmesinde etkili olduğu gösterilmiştir.
- Dirençli hipertansiyonu olan hastalarda, kantitatif PET ile tedavi etkinliğinin değerlendirilmesinde hiperemik MKA ve MAR farkı gösterilmiştir (102).
PET Miyokardiyal Perfüzyon Görüntüleme Raporlama Önerileri
Kardiyak PET gibi kompleks bir çalışma için doğru bir rapor formatı gerekmektedir. Tablo 2’de raporun içermesi gereken bulgular özetlenmiştir. Çalışma endikasyonunun, çalışmadan elde edilen çeşitli verilerin etkisini vurgulamak için raporda bulunmasına özellikle dikkat edilmelidir. Kantitatif PET verilerine verilen önem, radyofarmsötiğin tutulumunun görsel olarak değerlendirilmesinin önemini düşürmemektedir. AHA 17 segment sınıflamasına göre iskemik veya nekrotik segment sayısı, SRS, SSS ve SDS skorları ve iskemi yüzdesi detaylı olarak verilmelidir. Benzer şekilde, duvar hareket bozukluğu, istirahat ve stres SVEF değerleri raporlanmalıdır. Kantitatif PET verilerinde olduğu gibi, önceki raporlar ile karşılaştırma için, özellikle başka merkezli çalışma durumunda, kullanılan yazılım ve model gibi çalışmanın teknik yöntemleri elden geldiğince raporlamada belirtilmelidir. Yukarıda daha önce bahsedildiği gibi ve O-15 su dışında, hiperemik MKA ve MAR için farklı ajanlar ile sınır değerleri belirlenemediği için uygun referans verilerek dikkate alınan değerler belirtilmelidir. O-15 su çalışmalarında, görsel değerlendirmeye ilaveten yarı kantitatif skorlar ve Gated PET verileri eklenmelidir. O-15 su kullanan çeşitli gruplar, koroner alanda normal görsel perfüzyon görüntüleme verilerini, ardışık en az iki segmentte, MKA değeri desteklemiyor ve <2,3 mL/gr/dk ise anormal olarak sınıflamaktadır (65). Rapor, hibrit görüntüleme kullanılan merkezlerde kalsiyum skoru ve kardiyak BT anjiyografi ile ilgili verileri de içermelidir. Raporun sonuç kısmında tüm veriler, en önemlisi, klinik soruların cevaplanması için ilgili özel veriler belirtilmelidir. Özellikle en önemli nokta, dengeli üç damar miyokardiyal iskemi ve diffüz mikrovasküler hastalık ayrımını yapmaktır. Muhtemel kriterler arasında, perfüzyon defekti olmadan MKA’da homojen azalma daha çok mikrovasküler hastalığı işaret etmekte iken daha heterojen azalma KAH nedeni ile dengeli iskemiyi hatırlatıcı olarak görülmektedir.
PET Miyokardiyal Perfüzyon Görüntüleme İçin Ek Bilgiler
Hibrit Görüntüleme
Kardiyak hibrit görüntüleme, KAH tanısında anatomik ve fonksiyonel durumun birlikte değerlendirilmesi için değişik görüntüleme yöntemlerinin güçlü taraflarını birleştirme imkanı vermektedir (100,101,103). Bu işlev, hibrit tarayıcı veya farklı görüntüleme sistemlerinin yazılım tabanlı görüntülerinin birleştirmesi ile yapılabilmektedir. Koroner anatominin BT değerlendirmesini yapan çok detektörlü BT ile PET birleşimli hibrit tarayıcılar ticari olarak standart cihazlar olmaya başlamıştır. BT’ye ek olarak, yeni nesil tarayıcılarda PET ve MR birleşimini de görebilmekteyiz (103). Kardiyak BT anjiyografi (KBTA), birçok şüpheli KAH hastasında tanısal invaziv koroner anjiyografiye alternatif haline gelmiştir. Bu görüntüleme yöntemi koroner arter darlığını belirlemede invaziv koroner anjiyografi ile karşılaştırıldığında yüksek duyarlılığa (>%95) ve obstrüktif KAH dışlamada yüksek güvenilirliğe sahiptir (104). Ancak KBTA, koroner arter stenozunun hemodinamik sonuçları hakkında bilgi sağlayamayan morfolojik bir görüntüleme yöntemidir. Bu nedenle, KBTA ve miyokardiyal perfüzyon görüntülemeyi birleştiren hibrit görüntüleme, hemodinamik olarak anlamlı darlığı, anlamlı olmayan darlıktan ayırt etmede yardımcıdır. Ayrıca, BT ile KAH sınırlarının belirlenmesi miyokardiyal perfüzyon görüntülemenin tanısal ve prognostik değerini artırmaktadır (105,106,107). Hibrit görüntüleme miyokardiyal perfüzyon anormalliklerinin ve karşılık gelen koroner arterlerin belirlenebilmesi için BT ve miyokardiyal perfüzyon görüntüleme verilerinin doğru uzaysal hizalanmasını sağlamaktadır. Hibrit görüntüleme çalışmalarında ancak %50-60 olguda gerçek koroner arter anatomisi ile uyumlu standart miyokardiyal bölgesel dağılım olduğu görülmüş olup bu durumun değerlendirmede yanılgıya sebep olabileceği gözönünde bulundurulmalıdır (108).
Hibrit Görüntüleme Protokolleri
Hibrit görüntüleme oldukça yeni bir teknoloji olup hala hibrit görüntülemeden hangi hastaların yararlanacağı, farklı çalışma usullerinin en iyi şekilde nasıl birleştirilebileceği ve hibrit görüntülemenin maliyet analizinin netleşmesi gerekmektedir. Miyokardiyal perfüzyon görüntüleme ve KBTA, en az 64 detektörlü PET/BT tarayıcı ile tek seansta yapılmalıdır. Farklı olarak, elektron ışınlı BT veya BT ile elde edilen kontrastsız koroner kalsiyum skorlama perfüzyon görüntüleme ile birlikte elde edilebilir. Ardışık testlerde, perfüzyon görüntüleme sonrası KBTA veya KBTA sonrası perfüzyon görüntüleme, ilk testte kesin olmayan veya belirsiz bulgularda, bir seçenektir. Obstrüktif KAH ve mikrovasküler disfonksiyon ayırımının yapılabilmesi için perfüzyon görüntüleme ve KBTA’nın beraber yapılması gerektlidir. Düşük KAH olasılıklı hastalarda ilk önce için KBTA önerilir, Yüksek KAH olasılıklı veya KAH olduğu bilinen hastalar ise miyokardiyal perfüzyon değerlendirmeden daha çok yararlanacaktır (109). Hasta hazırlığı KBTA, koroner kalsiyum görüntüleme, miyokardiyal perfüzyon görüntülemelerin her biri için aynıdır (110). Beta (b)-bloker kullanımı, perfüzyon anormalliğinin yaygınlık ve şiddetini değiştirse de, bir çalışmada KBTA öncesi kalp hızını yavaşlatmak için b-blöker alan hastalarda PET perfüzyon görüntülemenin tanısal doğruluğunu koruduğu gözlenmiştir (111,112). Uygun endikasyon ve muhtemel kontrendikasyonlar, ilaç alerjisi gibi, BT ve PET çalışmaları için ayrı ayrı değerlendirilmelidir. Birleşmiş görüntüyü ve verileri incelemek için bağımsız anatomik ve fonksiyonel görüntü analizinden ayrı olarak analiz yapacak yazılım gerekmektedir. Hibrit görüntülerde, gözlemciler arası iyi bir uyum, tekrarlanabilirlik ve kısa işlemleme zamanı sağlayan bu konuya özgü kardiyak bileştirme yazılım paketleri ticari olarak hazır bulunmaktadır (113,114). Bu yazılım paketleri, otomatik/yarı otomatik olarak, koroner anatomi verileri ile miyokardiyal perfüzyon verilerini üç boyutlu yapılandırmakta, sonuç olarak hibrit üç boyutlu görüntüler elde edilmektedir. İki veri arasında solunuma bağlı uyumsuzlukları gidermek ve kalp pozisyonuna bağlı olarak veya EKG-gated ve gated olmayan verilerde ufak atım farkı nedeni ile oluşan yanlış hizalamalara engel olmak için kesitsel görüntülerin yeterli oranda üst üste binmesi ve bazen elle düzeltilmesi gerekmektedir (115).
Radyasyon Maruziyeti
Her iki tekniğin de iyonizan radyasyon kullanması nedeni ile hibrit PET/KBTA görüntüleme hasta radyasyon dozunu artırmaktadır. Step-and shoot protokolü EKG tetiklemeli tek kaynak 64 kesit BT tarayıcı ile, KBTA için alınan radyasyon dozu 2-5 mSv olarak
hesaplanmıştır (116). Koroner kalsiyum görüntüleme KBTA’ya göre hastaya daha az radyasyon eklemektedir (yaklaşık 1 mSv) (100,101). Genç hastalarda ve/veya tetkik tekrarı gerektiren hastalarda, hibrit PET/MR görüntüleme PET/BT’ye göre daha az radyasyon dozu vereceği için tercih edilebilir (103).
Klinik Çalışmalar
Yapılan validasyon çalışmaları obstrüktif KAH’ı tespitte kardiyak hibrit PET/BT görüntülemenin uygulanabilir ve yüksek tanısal doğruluğa sahip olduğu göstermektedir. Bir meta-analizde (12 tanısal çalışma ve toplamda 951 hasta) KAH tanısı için yapılan koroner anjiyografide en az %50 lüminal çap azalmasında hibrit KBTA ve SPECT, PET perfüzyon görüntüleme, veya MR ile tek başına KBTA ile karşılaştırılmıştır (117). Bu meta-analizde hibrit görüntüleme ile KBTA arasında hasta bazında toplam duyarlılık %91 ve %90; damar bazında %84 ve %89 bulunmuştur. Ancak, özgüllük açısından hibrit görüntüleme ile KBTA hasta bazında karşılaştırıldığında, hibrit görüntülemenin açıkça daha yüksek özgüllüğe sahip olduğu görülmüştür (%93 ve %66, damar bazında %95 ve %83). Damar bazında tam tanı koyma açısından da ılımlı bir iyileşme (AUC 0,97 vs. 0,92) bulunmuştur. Bu meta-analiz ve güncel çalışmaların kısıtlılığı, birçoğunun referans olarak invaziv FAR yerine anjiyografik darlık çapını kullanmasıdır. Yakın zamanda tek merkezli prospektif PACIFIC çalışmasında 208 hastada hibrit görüntüleme ile KBTA, SPECT perfüzyon görüntüleme, O-15 PET perfüzyon görüntüleme ve tüm damarlar için FAR ölçümü ile yapılan koroner anjiyografi karşılaştırılmıştır (118). Bu çalışmada, KBTA’ya fonksiyonel görüntüleme eklemenin özgüllüğü artırdığı, ancak yüksek yalancı negatifliğin tek tek görüntüleme yöntemlerine göre toplamda tanısal kazanç getirmediği saptanmıştır. Bununla birlikte şüpheli obstrüktif KAH için yapılan hibrit çalışmanın, görüntüleme yöntemlerinin hem tek tek yapılan hem de yan yana verilerinin değerlendirilmesini inceleyen çalışmalarda, yaklaşık üçte bir hastada sonucu değiştirdiği gözlenmiştir (119,120). Hibrit görüntülemenin tamamlayıcı bilgi sağladığı bir diğer hasta grubu konjenital koroner anomalidir ve koroner anjiyografi by-pass greft sonrası tekrarlayan göğüs ağrısı olan hastalardır (121,122). Ayrıca, hibrit görüntüleme obstrüktif KAH olmadan mikrovasküler disfonksiyonlu hastaları belirleyebilir (123). Bu çalışmalar hibrit görüntülemenin en büyük değerinin, KBTA’da görülen koroner anormalliğin hemodinamik anlamını değerlendirme, epikardiyal ve mikrovasküler hastalığın ayrımını yapma ve aynı zamanda iskemiye sebep olan lezyonu doğru tespit etmekte olduğunu göstermektedir. Daralmış koroner arter tarafından beslenen bölge ile uyumlu miyokardiyal iskemi, darlık olan damarla uyumlu olmayan iskemiye göre daha yüksek ölüm ve miyokardiyal enfarktüs riski taşımaktadır. Bir diğer çalışmada, O-15 su PET ile izlenen anormal stres MKA, KBTA’da izlenen stenoz ile uyum gösterdiği durumda yüksek ölüm riski, miyokardiyal enfarktüs veya unstabil anjina ile ilişkili bulunmuştur (124).
Koroner arter kalsiyum görüntüleme, ateroskleroz yükünü belirleyebilmesi nedeni ile, miyokardiyal perfüzyon görüntülemeye ek bilgi sağlamaktadır (125). Normal miyokardiyal perfüzyon görüntüleme bulgusu olan hastalarda yüksek ateroskleroz yükü, artmış obstrüktif KAH olasılığı ve ciddi kardiyak olay geçirme riski ile ilişkili bulunmuş olup sıfır koroner kalsiyum skoru, düşük risk grubundaki hastayı göstermektedir. Koroner arter kalsiyum skoru, bilinen KAH risk faktörlerine ek olarak koroner vasküler bozukluğu tahmin etmede, hiperemik MKA ve MAR ile ters ilişkilidir (126).
Hibrit PET/MR tarayıcılar teknik nedenlerden dolayı kısa süre önce kullanıma girmiştir. Farklı F-18 FDG uygulama protokolleri ile multimodalite PET/MR’nin, çoklu organ hastalığında kardiyak infiltrasyonun değerlendirilmesi, miyokardiyal canlılık tespiti ve enflamasyonun gösterilmesinde potansiyel rolü bulunmaktadır (127,128). Ancak, PET/MR tarayıcıları ile miyokardiyal perfüzyon görüntüleme ile ilgili deneyim sınırlıdır. Rb-82’nin PET/MR protokolü için kullanımı zordur, çünkü Rb-82 jeneratörü MR görüntüleme ile uyumlu değildir. F-18 flurpiridaz, miyokardiyal enfarktüslü bölgenin genişliğini tespit etmede, uzun yarı ömrü nedeniyle MR ve PET miyokardiyal perfüzyon çalışması için daha uygundur (129,130).
Yeni Ajan (F-18 Flurpiridaz)
Mitokondrial kompleks-1’e bağlanan F-18 flurpiridaz ile yapılan Faz 1 çalışmaları, bu ajanın klinik olarak güvenli ve kabul edilebilir dozimetrisi olduğunu; hem egzersiz treadmill testi ile hem de farmakolojik koroner vazodilatör stres testi ile yüksek kalitede görüntü sağladığını göstermektedir (131,132). Ön veriler MKA ve MAR’yi de içeren kantitatif değerlendirme kapasitesine sahip olduğunu göstermektedir (133). Bilinen veya şüpheli KAH olan hastalarda, tek gün istirahat/stres PET miyokart perfüzyon görüntüleme protokolünün etkinliğini geliştirmek ve değerlendirmek için bir Faz 2 çalışma (BMS747158-201) yapılmış ve PET miyokart perfüzyon görüntülemenin duyarlığı %76, özgüllüğü %74-87,7, SPECT miyokardiyal perfüzyon görüntüleme duyarlılığı %59,6-71,2, özgüllüğü %76,7-89 olarak bulunmuştur (134).
KAH hastası veya şüphesi olan, koroner anjiyografi için gönderilen hastalarda F-18 flurpiridaz PET miyokart perfüzyon görüntüleme ile SPECT miyokardiyal perfüzyon görüntülemenin karşılaştırıldığı, intrakoroner anjiyografinin altın standart olarak kabul edildiği Faz 3 (BMS747158-301 (ClinicalTrials.gov Identifier: NCT01347710) çalışmada; hastalara tek gün istirahat/stres protokolü uygulanmış ve F-18 flurpiridaz PET miyokardiyal perfüzyon görüntülemenin SPECT miyokardiyal perfüzyon görüntülemeye duyarlılıkta (p<0,001) anlamlı üstünlüğü gösterilmiş olmasına rağmen özgüllük açısından %76,2’ye %86,8 olarak bulunmuştur. F-18 flurpiridazın klinik kullanımı için yapılan başka bir faz 3 kohort çalışmasında (AURORA, ClinicalTrials.gov Identifier: NCT03354273), bulunan kantitatif stres MKA değerlerinin, hasta bazlı ve damar bazlı KAH tanısını doğru olarak belirleyebildiği gösterilmiştir (135).
Sonuç
PET miyokart perfüzyon sintigrafisi, KAH olan hastalarda hemodinamik açıdan önemli koroner arter darlığının değerlendirilmesinde yüksek tanısal performansı sayesinde altın standart olarak kabul edilmektedir. Uzun yıllardır anlamlı koroner arter darlığının neden olduğu miyokart iskemisinin varlığını tespit etmek için SPECT miyokart perfüzyon sintigrafisi önemli bir yöntem olmuştur. Ancak, dengeli hipoperfüzyonun varlığını ve ciddiyetini belirlemede yetersiz kalmıştır. PET miyokart perfüzyon sintigrafisi, MKA’yı kantitatif olarak ölçebilme yeteneği sayesinde mikrovasküler dolaşım bozukluğunu erken safhalardan itibaren tespit edebilir. Bu sayede tanı alamadıkları veya yetersiz tedavi gördükleri için prognozu kötü seyreden hastaların tespitine yardımcı olabilir. Günümüzde, gelişen teknolojiye paralel olarak kullanıma giren PET/BT ve PET/MR gibi hibrit görüntüleme modaliteleri, hem anatomik hem fonksiyonel bilgilerin birarada elde edilebilmesine olanak sağlamakta, böylece yöntemin tanısal doğruluğunu ve prognostik değerini de artırmaktadır. Ayrıca yeni geliştirilen uzun ömürlü, kolay ulaşılabilir PET radyofarmasötikleri sayesinde de yakın gelecekte PET miyokart perfüzyon sintigrafisinin klinik pratikte yerini alması beklenmektedir.